トレーサビリティの確保された新規血液製剤情報収集システム(J-HeST)について
目的
輸血の安全性の向上と適正使用の実現のために、日本赤十字社がもつデータと医療施設のもつデータを血液バッグの製造番号を介して連結することで、血液製剤の製造から使用までのBlood transfusion chainを追跡できるトレーサビリティの確保されたシステムを新規に構築しました。このシステムによりtransfusion chainがシームレスにつながることで、輸血に関連する様々なイベントを評価・解析可能となり、日本における輸血の安全性向上と適正使用につながる情報の大規模な収集と活用が期待されます。
システムの流れ
① 登録
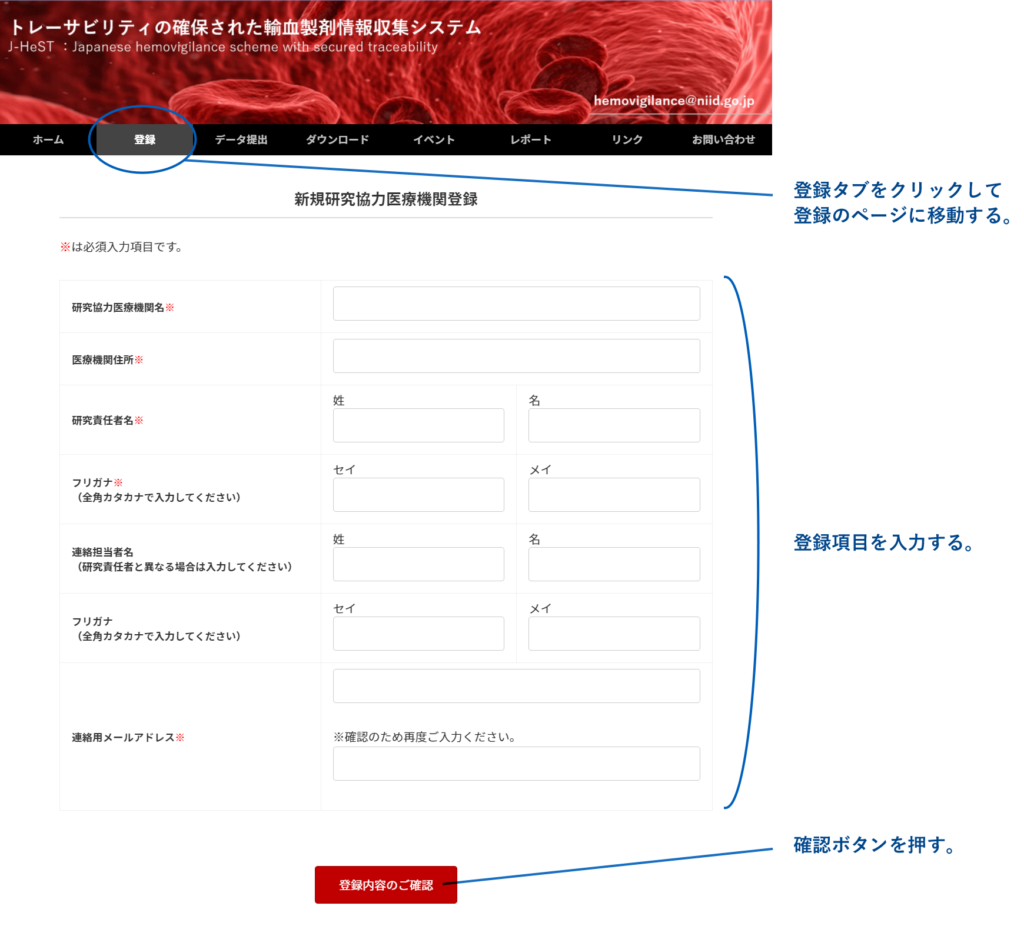
- ホームページの「登録」タブをクリックいただき、研究協力機関登録ページに移動してください。
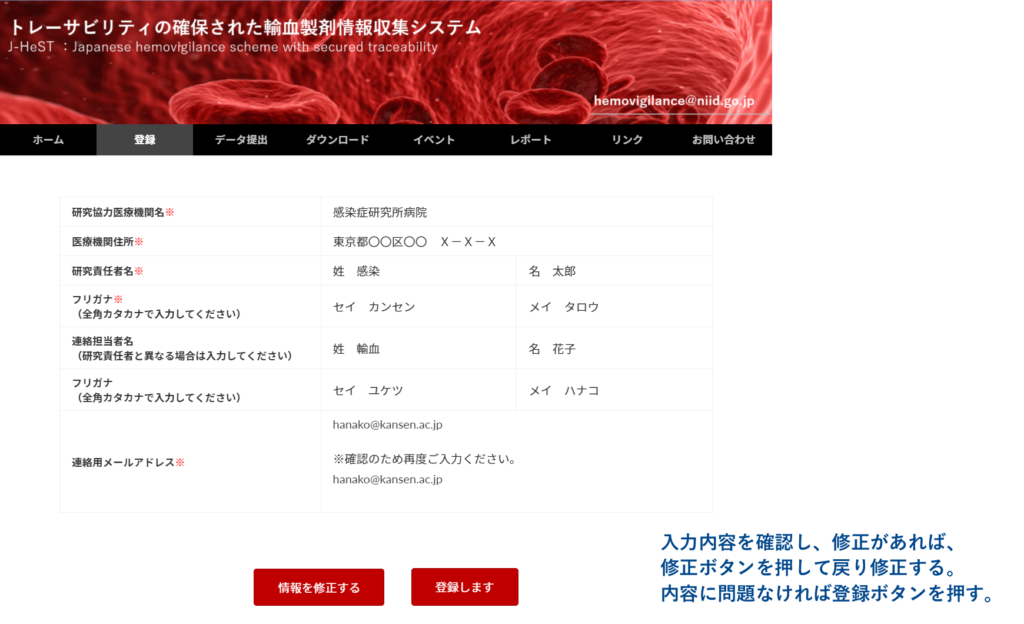
- 登録情報[医療機関名(フリガナ)、病院住所、研究責任者名(フリガナ)、連絡担当者名(フリガナ)、連絡用メールアドレス]を入力し、内容確認ボタンを押してください。
- 入力内容を確認し、登録ボタンをクリックしてください。
- システムよりオートリプライで連絡先e-mailに返信されます。
- 後日、システム担当者より登録確認のメールが担当者のe-mailに送信されて登録完了となります。
② 輸血に関するデータ作成
- ダウンロードページに移動し、データ作成用ファイル3点をダウンロードしてください。
- 「データシート(チェック機能つき)」
- 「データ定義書」
- 「データチェック操作手順書」
- 収集データ項目は、
- 輸血製剤の情報…製剤番号、製剤の種類(RBC, PC, FFP)、製剤有効期限日、納品日、接続前照合(投与開始)日、もしくは廃棄日
- 受血者の情報…年齢、性別、血液型(ABO、Rh)、施設洗浄の有無、輸血関連副反応の有無、副反応有の場合その症状、診断(「輸血副反応の症状項目ならびに診断項目表」に基づいた分類)、重症度レベル、輸血関連性
- 各データ項目について、「データ定義書」の内容に従って、「データシート(チェック機能つき)」にデータを入力してください(輸血管理システムからの出力データをシートに取り込んでください)。
- 「データチェック操作説明書」に従って、「データシート(チェック機能つき)」に入力したデータのチェックを行ってください。
- 任意入力の項目以外でチェックによりエラーとなった項目については修正をしてください。
- 修正後、データチェックしてエラーが修正されたことを確認してください。
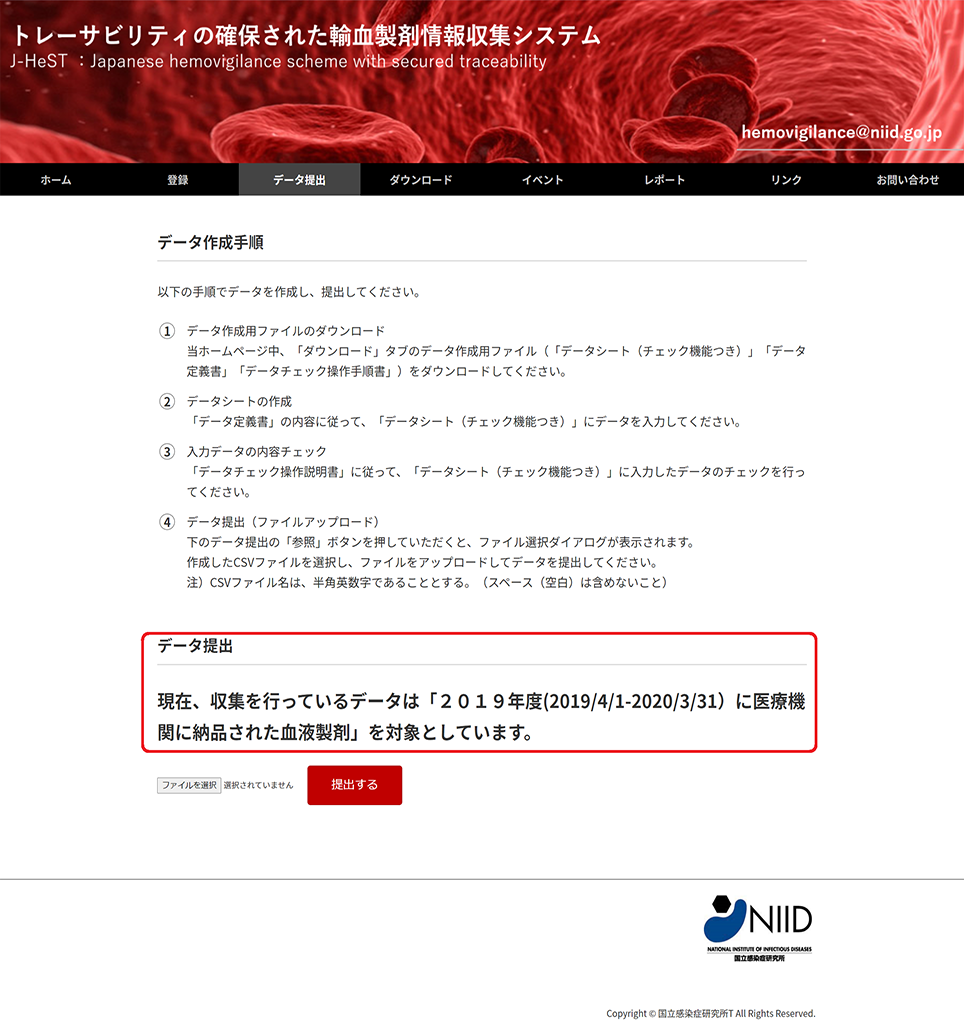
③ 作成したデータの提出
- データ提出ページに移動していただき、「参照」ボタンを押していただくと、ファイル選択ダイアログが表示されます。作成したファイルを選択し、アッロードしてデータを提出してください。
- データの修正が必要な場合は、修正したデータを同様にアップロードすると、該当する製剤の製造番号のデータに上書き保存されます。
- 製造番号の修正、データの削除が必要な場合は、システム担当者にご連絡ください。
<データ提出期間について>
データの提出期間は、原則、毎年8月〜12月にお願いします。それ以外の時期の提出も可能ですので、担当者にご相談ください。
提出いただくデータは、その前年のデータになります。
(例)データの提出日が、2021年9月1日の場合、2020年1月1日〜2020年12月31日に医療機関に納品された血液製剤についてデータシートを作成してください。
オンタイムで収集しているデータの期間をデータ提出ページに記載しています。
該当期間のデータを提出してください。
④ 収集データを使用した研究について
収集したデータについては国立感染症研究所にて解析し、適宜、日本輸血細胞治療学会等にて報告する他、ホームページのレポートのページにアップロードしていく予定です。
将来的に、多くの研究者が収集データを活用できるような環境を整備したいと考えています。決まり次第、ホームページにてアナウンスしたいと思います。
2021年7月20日 第1版
国立感染症研究所
システム担当:松岡佐保子